亚硫酸钠是怎样生产的? 硫酸钠生产工艺
网上有很多关于亚硫酸钠是怎样生产的?的问题,也有很多人解答有关硫酸钠生产工艺的知识,今天艾巴小编为大家整理了关于这方面的知识,让我们一起来看下吧!
内容导航:
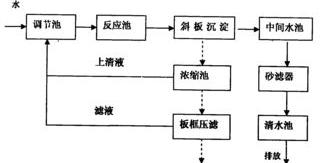
一、亚硫酸钠是怎样生产的?
由于盐酸比亚硫酸酸性大,氯化氢可以与亚硫酸钠反应得到二氧化硫,从而将氯化氢从二氧化硫中脱除;
但实际上,饱和亚硫酸钠溶液也能吸收二氧化硫:
因此,用饱和亚硫酸钠溶液脱除二氧化硫中的氯化氢会造成二氧化硫的损失,应使用饱和亚硫酸氢钠溶液代替饱和亚硫酸钠溶液,饱和亚硫酸钠溶液不与二氧化硫反应,但能与氯化氢反应:
最后提醒一句:饱和亚硫酸氢钠溶液的配制可以用市售的亚硫酸氢钠(NaHSO3)试剂或焦亚硫酸钠(Na2S2O5)试剂溶于水,效果是一样的,因为焦亚硫酸钠溶于水可再生亚硫酸氢钠:
市售的亚硫酸氢钠试剂或焦亚硫酸钠试剂实际上是Na2SO5和Na2SO3的混合物。这是因为当亚硫酸氢钠从溶液中结晶出来时,容易发生分子间脱水反应,得到焦亚硫酸钠。有些资料甚至认为固态根本没有Na2SO5,只有Na2SO5存在,Na2SO3只存在于溶液中。
饱和亚硫酸氢钠溶液通常不是完全无色的,它常常是淡黄色甚至黄绿色。
二、焦亚硫酸钠的生产工艺
焦亚硫酸钠俗称:重硫重氧。
分子式:Na2S2O5
分子量:190.1从0
理化性质:焦亚硫酸钠为白色或黄色结晶360问答粉末或小晶体,有强烈的SO2气味,比限量或产品重量重1.4。它溶于水,水溶液呈酸性。当它与强酸接触时,会释放出SO2生成相应的盐类,在空气中放置时间长了,就会被氧化成Na2SO4,所以产品不能长时间保存。150C以上,SO2分解。
焦亚硫酸钠是一种广泛使用的产品。
主要用于医药原料、板到李造纸漂白、照相、印刷显影、吃丝除味剂、皮革铬鞣剂、染料、印染、纺织染色助剂、棉絮、表里革剥色机染纤维漂白、脱氯剂、含铬废水处理剂、化学工业中的有机合成氧化还原剂、橡胶乳液处理剂、食品酿造、工作条件下的防结块和快速漂白、防腐。自建厂以来,产品的销售对象已从最初的特斯所开创的制药、染料行业发展到化工、食品、摄影行业的基础原料,以及竹制品的过蛾漂白、三废处理球套、水处理应用、建筑应用制造低肥力混凝土减水剂。
焦亚硫酸钠技术指标对照表
项目
国家行业标准
企业内部控制标准
高级产品
高级产品
主含量(以Na2S2O5计)
铁(以Fe计)含量
水不溶物含量
砷(As)含量
上海化工产品质量监督检验中心检验报告
检查结果总结
序列号
检验项目
试验结果
主要含量(以Na2S2O5计),%
铁(以Fe计)含量,%
水不溶物含量,%
砷(砷),%
重金属(以铅计算),%
氯化物(Cl),%
透明度%
有资格的
硫酸盐(SO4),%
三、硫代硫酸钠合成的工艺流程 附图
(1)fes2与o2反应生成氧化铜和二氧化硫,反应的化学方程式为4fes2 11o2高温. 2fe238so2,故答案为:4fes2 11o2高温. 2 Fe 238 so 2;(2)从工艺中使用的原料和生产工艺可知,从经济效益、工艺简单、无污染等因素来看,那氯气用在A、B、C中,硫化氢用在C中就是有毒气体。甲中盐酸和氢氧化物研磨的原理价格昂贵,丙中制备氯气的原料碳酸钠价格昂贵;第二种原料丰富,价格低廉,工艺简单,所以答案是:B;工艺B中的原料fes2来源丰富,价格低廉,仿制工艺简单,技术成熟;(3) (1)用乙醇润湿硫磺粉,便于硫磺被水浸湿,干燥反应接触面积,增加反应速率,提高反应物利用率。如果加入的硫磺粉没有被乙醇润湿,会降低反应速率,降低产品收率;(A)如果硫磺粉不被乙醇润湿,反应速率会降低,所以A是正确的;(B)反应条件是用小火将硫磺粉加热至微沸点,不需要用乙醇润湿硫磺粉就可以提高反应温度,故B错误;(C)硫磺粉没有被乙醇润湿,对溶液的ph值没有影响,所以反应体系的ph值没有变化,故C错误;(D)硫磺粉反应得到的产物较少,会降低产量,故D正确;所以答案是:ad;(2)溶液中获得晶体的操作是蒸发浓缩,冷却结晶,1060g,冷却至10,过滤洗涤析出的晶体,干燥得到所需晶体,从而获得na2s2o3?5h2o结晶,所以答案是:蒸发、浓缩、冷却至10结晶、过滤;亚硫酸钠在加热过程中容易氧化成硫酸钠;根据硫酸根离子的测试方法,设计实验进行验证和判断。实验方法如下:取出少许滤液置于试管中,加入稀盐酸至溶液呈酸性,然后过滤得到S,再向滤液中加入bacl2溶液。如果有白色沉淀,可以证明含有na2so4,所以答案是:na2so 4;取出少许滤液,置于试管中,加入稀盐酸至溶液呈酸性,过滤得S,再向滤液中加入bacl2溶液,若有白色沉淀,则可证明含有na2so4;如果这个反应完全得到Na2S2O3: m (Na2S2O3)=15.1g 158g?mol?1126g?mol?1=18.9g,若蒸发浓缩得到的30ml溶液为饱和溶液,其na 2 S2 o 3:m(na 2 S2 o 3)=30ml1.2g/cm3200g 200g=24g,且18.9g<24g,则该溶液不饱和,70无晶体析出,则答案为:mol?1126g?mol?1=1=18.9g .若蒸发浓缩得到的30ml溶液为饱和溶液,其na 2 S2 o 3:m(na 2 S2 o 3)=30ml1.2g/cm3200g 200g=24g,且18.9g<24g,则该溶液不饱和,70无晶体析出。
以上就是关于亚硫酸钠是怎样生产的?的知识,后面我们会继续为大家整理关于硫酸钠生产工艺的知识,希望能够帮助到大家!
推荐阅读
- alfa romeo车标含义?(阿尔法罗密欧车标)
- 华为鸿蒙os如何操作 华为鸿蒙os2.0系统官网报名入口
- 14款沃尔沃s60l二手车能买吗?(沃尔沃s60为什么贬值厉害)
- power mp3 wma converter(mp3格式转换器)软件介绍(power mp3 wma converter(mp3格式转换器))
- 42岁李贞贤宣布平安生女,网友:歌声击退山贼的那个
- 热火朝天的高铁WiFi迟迟未到(5G能否破局)
- 华为手机性价比最高是哪几款2022? 华为哪款手机性价比高最值得入手
- 进口捷豹全部车型报价?(捷豹报价大全价格表)
- 韩庚江铠同疑相恋,两人同游马尔代夫遭曝光
- 八卦格字帖软件介绍(八卦格字帖)
- 虚拟机 操作系统(操作系统整合:虚拟机管理程序的下一步)
- 比亚迪f6参数配置?(比亚迪f6)
- 奥沙利文获世锦冠军,奥沙利文得了几次世锦赛冠军
- Evel Knievel手游游戏介绍(Evel Knievel手游)
- 索尼wi1000x拆解(SONYNZW-X1000系列高清拆解图集)
- 4座硬顶敞篷跑车都有哪几款?(4门4座硬顶敞篷车推荐)
- 艺术体操团体全能决赛,艺术体操团体全能决赛中国
- 工人物语6通用修改器游戏介绍(工人物语6通用修改器)
- 简述电机换向器的工作原理图(简述电机换向器的工作原理)
- Atheros-AR5007EG无线网卡驱动软件介绍(Atheros-AR5007EG无线网卡驱动)
